Otimizando a seleção de pacientes para atezolizumabe adjuvante em CPNPC ressecado

Análise exploratória do ensaio IMpower010, apresentada no ESMO Immuno-Oncology Congress 2021, confirma que há uma correlação entre a expressão de PD-L1 em células tumorais e a sobrevida livre de doença em pacientes com CPNPC
O estudo IMpower010 (NCT02486718) demonstrou no início de 2021 que o atezolizumabe aumentou a sobrevida livre de doença (SLD) em comparação aos cuidados de suporte padrão (CSP) em pacientes com câncer de pulmão não pequenas células (CPNPC) estádio II-IIIA. Os pacientes foram estratificados pela expressão de PD-L1 determinada por SP142.
Na ESMO Immuno-Oncology Congress 2021, foram apresentados os resultados de SLD por subgrupo de expressão de PD-L1 nas células tumorais por outra análise imuno-histoquímica, a SP263, entre 859 pacientes avaliáveis com doença estádio II-IIIA. Observou-se que o atezolizumabe foi superior em comparação aos CSP em todos os subgrupos com PD-L1 positivo:
PD-L1 ≥ 1%: HR 0,66; IC 95% 0,49–0,87
PD-L1 1–49%: HR 0,87; IC 95% 0,60– 1,26
PD-L1 TC ≥ 50%: HR 0,43; IC 95% 0,27–0,68
Não houve diferença de SLD entre atezolizumabe e CSP em pacientes com PD-L1 < 1% (HR 0,97; IC 95% 0,72–1,31). Ao serem excluídos aqueles com alteração em EGFR/ALK, ganhos numéricos em SLD foram observados em todos os subgrupos (tabela 1):
PD-L1 < 1%: HR 0,92;
PD-L1 ≥ 1%: HR 0,62;
PD-L1 1–49%: HR 0,82;
PD-L1 ≥ 50%: HR 0,43;
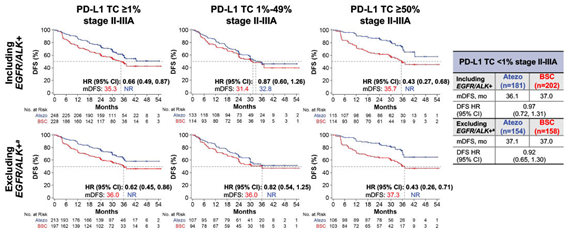
Tabela 1: Curvas de Kaplan-Meyer avaliando a SLD em pacientes com CPNPC, com ou sem alteração em EGFR/ALK, de acordo com a expressão de PD-L1 por SP263. Fonte: ESMO Immuno-Oncology Congress 2021, Abstract 2º.
Os resultados demonstram que o uso de SP263 para atribuir pacientes aos diferentes subgrupos de expressão de PD-L1 se compara a estratificação original determinada por SP142. Observa-se, inclusive, uma correlação entre a expressão de PD-L1 em células tumorais e a SLD – as alterações oncogenéticas provavelmente são marcadores desfavoráveis para o uso de atezolizumabe nesta população.
A análise também avaliou DNA tumoral circulante (ctDNA) após a cirurgia. Entre 534 pacientes, a positividade do ctDNA aumentou de acordo com o estádio da doença (14% tinham CPNPC estádio II; 29% estádio IIIA). A positividade do biomarcador associou-se a um pior prognóstico; entre os pacientes que receberam CSP, a mediana de SLD foi de 7,9 meses para aqueles com ctDNA-positivos e não foi alcançada para os negativos. O atezolizumabe aumentou a SLD em comparação aos CSP em pacientes ctDNA-negativos e ctDNA-positivos, observando-se maior benefício para o subgrupo PD-L1 ≥ 1%.
Os autores concluem que as análises confirmam que há uma correlação entre a expressão de PD-L1 em células tumorais e a sobrevida livre de doença em pacientes que receberam atezolizumabe para tratamento de CPNPC estádio II-IIIA, e que o benefício do anti-PD-L1 sobre CSP também foi observado tanto em pacientes ctDNA-positivos quanto negativos, porém maior no subgrupo PD-L1 ≥ 1%.
Referências:
- Zhou C, et al. IMpower010: biomarkers of disease-free survival (DFS) in a Phase 3 study of atezolizumab (atezo) vs best supportive care (BSC) after adjuvant chemotherapy in stage IB-IIIA NSCLC. ESMO Immuno-Oncology Congress 2021, Abstract 2O.