Presença e impacto de anticorpos antidrogas (ADAs) nos desfechos de pacientes do estudo HIMALAYA

Os resultados da análise dos ADAs para tremelimumabe e durvalumabe no estudo HIMALAYA demonstram que há um baixo risco de ADAs para o tratamento do carcinoma hepatocelular irressecável com o protocolo STRIDE ou durvalumabe em monoterapia. As taxas de ADAs emergentes do tratamento e anticorpos neutralizantes para tremelimumabe e durvalumabe foram baixas (≤11%). A presença de ADAs não pareceu afetar a eficácia clínica ou a segurança da monoterapia STRIDE ou D no pequeno número de pacientes que foi positivo para ADA
Hoje na clínica, o uso de inibidores de checkpoint imunológico faz parte do tratamento padrão de muitos tipos de tumores. Anticorpos monoclonais humanizados e totalmente humanos contra PD-L1 ou PD-1 tiveram o maior sucesso até o momento, com cinco medicamentos aprovados (nivolumabe, pembrolizumabe, atezolizumabe, durvalumabe e avelumabe). Nos últimos anos muitos ensaios com desenhos muito semelhantes foram conduzidos com essas drogas e, embora seus alvos sejam semelhantes, existem algumas discrepâncias nos resultados. Uma justificativa para essas discrepâncias é resultado da atuação do sistema imunológico.
Qualquer agente biológico administrado a humanos provavelmente será reconhecido pelo sistema imunológico que induz uma resposta humoral resultando na geração de anticorpos antidrogas (ADAs). Esses anticorpos podem se ligar ao fármaco e causar perda de atividade por diferentes mecanismos, como bloqueio da ligação ao alvo do fármaco (anticorpos neutralizantes) ou aumento da depuração do complexo ADA-fármaco, resultando em concentrações plasmáticas reduzidas do fármaco. Além disso, os ADAs podem induzir toxicidades pela geração de uma resposta imune ao complexo ADA-fármaco, sendo as reações relacionadas à infusão os eventos mais frequentes. Estudos anteriores relataram que os ADAs podem diminuir a atividade antitumoral dos inibidores de checkpoint imunológico no carcinoma hepatocelular. As taxas relatadas de ADAs emergentes do tratamento (TE-ADAs) variam de 1,5% para pembrolizumabe e 8,6% para nivolumabe a 54,1% para atezolizumabe em todas as indicações.
Durante o 2023 ASCO GI Cancers Symposium foram apresentaram os resultados da análise dos ADAs para tremelimumabe (T) e durvalumabe (D) no estudo HIMALAYA. O estudo global, aberto, de fase 3 HIMALAYA (NCT03298451) mostrou que o protocolo STRIDE (Single Tremelimumab Regular Interval Durvalumab), que consiste em uma dose inicial única e alta de tremelimumabe (anti-CTLA4) mais durvalumabe (anti-PD-L1), melhorou significativamente a sobrevida global em comparação com sorafenibe (S). Ainda, o estudo demonstrou que a monoterapia com durvalumabe não foi inferior ao sorafenibe em pacientes com carcinoma hepatocelular irressecável (uHCC).
As análises secundárias pré-especificadas avaliaram a presença de ADAs para D e T antes da primeira dose do estudo (basal), uma vez durante o tratamento e uma vez após a descontinuação do tratamento. Para os pacientes que eram positivos para ADA em qualquer visita (ADA+), a presença de anticorpos neutralizantes (nAbs) também foi avaliada. TE-ADA+ foi definido como pacientes com uma amostra pós-basal positiva apenas ou pacientes com um título de ADA que aumentou ≥4 vezes após o tratamento. ADA negativo (ADA–) foi definido como pacientes sem amostra positiva em qualquer visita, na linha de base ou pós-linha de base. Taxa de resposta objetiva (ORR; RECIST v1.1, inc. não confirmado), sobrevida global (SG) e eventos adversos relacionados ao tratamento (TRAEs) foram avaliados em subgrupos de ADA.
A frequência de ADAs para D foi semelhante nos braços STRIDE (T+D) e D: 8,2% (24/294) e 7,1% (20/282) dos pacientes, respectivamente, eram ADA+ para D; 3,1% (9/294) e 2,8% (8/282) dos pacientes, respectivamente, eram TE-ADA+ para D; e 1,7% (5/294) e 0,7% (2/282) dos pacientes, respectivamente, tinham nAbs para D. No braço STRIDE, 15,9% (29/182) dos pacientes eram ADA+ para T; 11,0% (20/ 182) dos pacientes eram TE-ADA+ para T, e 4,4% (8/182) dos pacientes tinham nAbs para T. Embora o número de pacientes fosse pequeno, no braço STRIDE, a ORR foi de 11,1% (1/9) em pacientes TE-ADA+ a D, 35,0% (7/20) em pacientes TE-ADA+ a T e 23,9% (94/393) no conjunto de análise completo (FAS). No braço D, a ORR foi de 25,0% (2/8) nos pacientes TE-ADA+ a D e 18,5% (72/389) no FAS. A SG para pacientes TE-ADA+/nAb+ para D ou T nos braços D e STRIDE foi consistente com o FAS. Em ambos os braços, as taxas de TRAE e TRAE de Grau 3/4 não aumentaram nos grupos ADA+ vs ADA– (Tabela) e foram geralmente consistentes com a população geral.
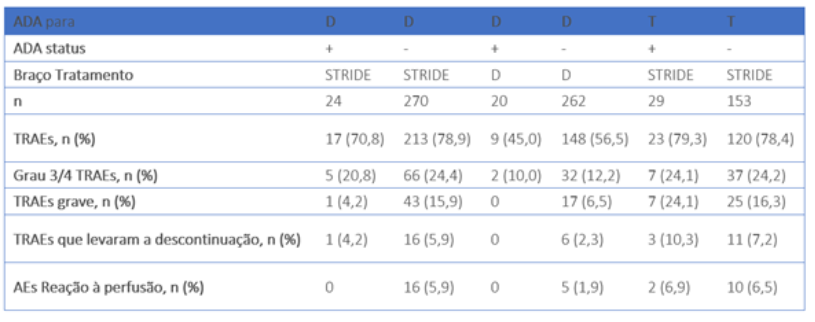
Os autores concluíram que no HIMALAYA, as taxas de TE-ADAs e nAbs para D e T foram baixas (≤11%). A presença de ADAs não pareceu afetar a eficácia clínica ou a segurança da monoterapia STRIDE ou D no pequeno número de pacientes ADA+. Esses resultados suportam um baixo risco de ADAs para STRIDE ou D em uHCC.
Referências:
1 – CRYSLER, Oxana V. et al. Presence and impact of antidrug antibodies (ADAs) to tremelimumab (T) or durvalumab (D) in the phase 3 HIMALAYA study of unresectable hepatocellular carcinoma (uHCC). J Clin Oncol 41, 2023 (suppl 4; abstr 551)
2 – ABOU-ALFA, Ghassan K. et al. Tremelimumab plus Durvalumab in Unresectable Hepatocellular Carcinoma. NEJM Evidence, p. EVIDoa2100070, 2022.
3 – ENRICO, Diego et al. Antidrug Antibodies Against Immune Checkpoint Blockers: Impairment of Drug Efficacy or Indication of Immune Activation? Immunogenicity of Cancer Immunotherapy. Clinical Cancer Research, v. 26, n. 4, p. 787-792, 2020.
© 2020 Oncologia Brasil
A Oncologia Brasil é uma empresa do Grupo MDHealth. Não provemos prescrições, consultas ou conselhos médicos, assim como não realizamos diagnósticos ou
tratamentos.


 Vea MedIQ en Español
Vea MedIQ en Español