Anvisa aprova uso de cemiplimabe para tratamento do carcinoma basocelular
Medicamento já era utilizado no manejo do carcinoma cutâneo de células escamosas e, agora, também pode ser empregado como recurso terapêutico no carcinoma basocelular (CBC) localmente avançado ou metastático
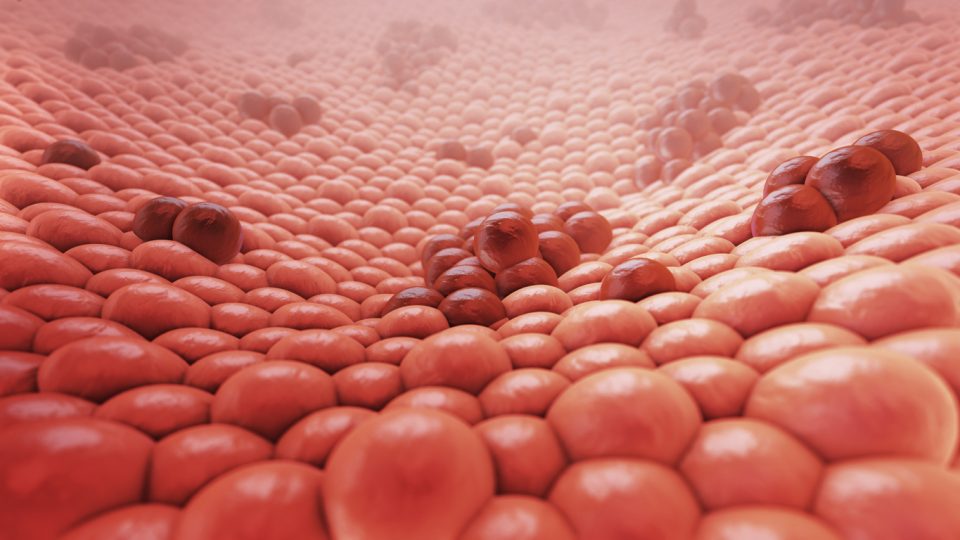
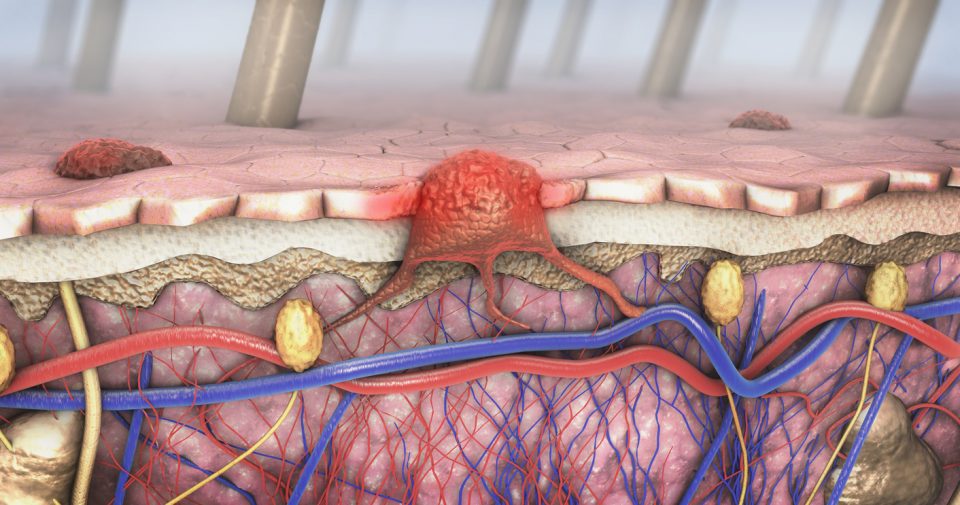
Neste dia 22 de março, a Agência Nacional de Vigilância Sanitária (Anvisa) aprovou o uso do inibidor de PD-1 cemiplimabe para tratamento do carcinoma basocelular (CBC) localmente avançado ou metastático previamente tratado com inibidor da via Hedgehog ou para os quais um inibidor da via Hedgehog não é adequado.
O anticorpo monoclonal, que já era usado, no Brasil, desde 2019, contra o carcinoma cutâneo de células escamosas, foi aprovado recentemente pela Food and Drug Administration (FDA), nos Estados Unidos. A liberação se baseou no mesmo estudo, um ensaio clínico aberto, multicêntrico e não randomizado de fase II.
Participaram 112 portadores de carcinoma basocelular localmente avançado ou metastático. A condição para se voluntariar era já ter progredido anteriormente com inibidor da via Hedgehog (IHH), não ter obtido resposta objetiva após nove meses de terapia com a droga ou ser intolerante a ela.
Todos os voluntários receberam 350 mg cemiplimabe intravenoso, a cada 21 dias, por, no máximo, 93 semanas.
Após a análise, os cientistas constataram que, nos 28 pacientes com câncer metastático, a taxa de resposta objetiva (TRO) foi de 21%. Já entre os 84 portadores do tumor localmente avançado, a TRO atingiu 31%. Em todos os participantes, a resposta foi mantida por, pelo menos, seis meses.
Os eventos adversos mais frequentes foram cansaço, dor musculoesquelética, diarreia, erupção cutânea, coceira e infecção do trato respiratório superior, observados em 15% dos indivíduos. Reações mais graves, como infecção do trato urinário, colite, lesão renal aguda, insuficiência adrenal, anemia e sonolência ocorreram em 32% dos casos.
A aprovação do cemiplimabe representa um avanço por trazer mais uma opção de tratamento contra o carcinoma basocelular em pacientes que não toleram o IHH ou não obtêm resultados com ele.
Referências:
- Lewis K,et al. 428 Interim analysis of Phase 2 results for cemiplimab in patients with metastatic basal cell carcinoma (mBCC) who progressed on or are intolerant to hedgehog inhibitors (HHIs). Abstract 8. 2020 Journal for ImmunoTherapy of Cancer.
DOI: 10.1136/jitc-2020-SITC2020.0428